Thông tư 32: Quy định về báo cáo theo dõi của cơ sở kinh doanh dược
Đây là quy định đáng chú ý được ban hành tại Thông tư 32/2018/TT-BYT quy định việc đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
Theo đó, Điều 5 Thông tư 32/2018/TT-BYT quy định cơ sở kinh doanh dược, cơ sở khám bệnh, chữa bệnh phải thực hiện việc theo dõi, giám sát, thu thập, tổng hợp, đánh giá và báo cáo cơ quan quản lý nhà nước có thẩm quyền thông tin các trường hợp phản ứng sau tiêm chủng, phản ứng có hại của thuốc theo quy định tại Điều 77, Điều 78 Luật dược, hướng dẫn Thực hành tốt cảnh giác dược (Good Pharmacovigilance Practices), các hướng dẫn quốc gia về cảnh giác dược và các quy định có liên quan.

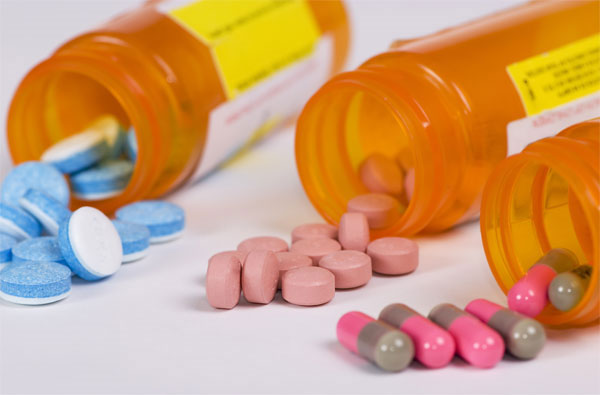
Hình minh họa (nguồn internet)
Ngoài ra, cơ sở đăng ký thuốc phải báo cáo đánh giá an toàn, hiệu quả đối với thuốc quy định tại khoản 2 Điều 8 Thông tư này theo Mẫu 2A/TT (đối với thuốc) hoặc Mẫu 2B/TT (đối với vắc xin):
-
Định kỳ 06 tháng một lần trong thời hạn giấy đăng ký lưu hành còn hiệu lực gửi về Trung tâm DI &ADR Quốc gia để tổng hợp, đánh giá và báo cáo Cục Quản lý Dược;
-
Khi nộp hồ sơ đăng ký gia hạn giấy đăng ký lưu hành tại Cục Quản lý Dược.
Thông tư 32/2018/TT-BYT nhấn mạnh quy định cơ sở khám bệnh, chữa bệnh có sử dụng thuốc báo cáo tình hình sử dụng thuốc theo Mẫu 2C/TT (đối với thuốc) ban hành kèm theo Thông tư này định kỳ 06 tháng một lần trong thời hạn giấy đăng ký lưu hành còn hiệu lực đối với thuốc quy định tại khoản 2 Điều 8 Thông tư này và gửi về Trung tâm DI & ADR Quốc gia để tổng hợp, đánh giá và báo cáo Cục Quản lý Dược.
Xem thêm quy định khác tại Thông tư 32/2018/TT-BYT có hiệu lực từ 01/9/2019.
Thu Ba
- Từ khóa:
- Thông tư 32/2018/TT-BYT
- Luật dược
- Tiếp tục hoàn thiện Nghị quyết về đổi mới Chương trình giáo dục mầm non
- Bảo đảm công tác khám chữa bệnh, cấp cứu TNGT trong dịp nghỉ lễ 30-4 và 1-5 năm 2024
- Yêu cầu kỹ thuật công tác thăm dò cát, sỏi lòng sông và đất, đá làm vật liệu san lấp từ ngày 06/6/2024
- Công khai thông tin về kế toán viên hành nghề từ ngày 01/7/2024
- Đề xuất sửa đổi quy định đối tượng tham gia bảo hiểm thất nghiệp
- Đề xuất chính sách hỗ trợ người lao động đi làm việc ở nước ngoài theo hợp đồng
-

- Áp dụng tiêu chuẩn chất lượng trong kiểm nghiệm ...
- 14:42, 25/01/2020
-

- 04 tiêu chí được miễn giai đoạn thử thuốc trên ...
- 09:37, 21/03/2019
-
.jpg)
- Thông tư 32: Hướng dẫn thủ tục cấp giấy đăng ký ...
- 09:25, 16/11/2018
-
- TH thẩm định nhanh hồ sơ nhập khẩu thuốc chưa ...
- 09:03, 16/11/2018
-

- Hướng dẫn thủ tục gia hạn giấy đăng ký lưu hành ...
- 09:16, 15/11/2018
-

- Tiếp tục hoàn thiện Nghị quyết về đổi mới Chương ...
- 08:01, 24/04/2024
-

- Bổ sung quy định về yêu cầu kỹ thuật công tác ...
- 17:18, 23/04/2024
-

- Phân loại và nguyên tắc sử dụng hệ thống tài khoản ...
- 17:12, 23/04/2024
-
- Bảo đảm công tác khám chữa bệnh, cấp cứu TNGT ...
- 17:00, 23/04/2024
-

- Yêu cầu kỹ thuật công tác thăm dò cát, sỏi lòng ...
- 16:30, 23/04/2024
 Mục lục bài viết
Mục lục bài viết
