Trình tự, thủ tục cho phép áp dụng chính thức kỹ thuật mới trong KCB
Thông tư 07/2015/TT-BYT quy định chi tiết điều kiện, thủ tục cho phép áp dụng kỹ thuật mới, phương pháp mới trong khám, chữa bệnh do Bộ trưởng Bộ Y tế ban hành ngày 03/04/2015.

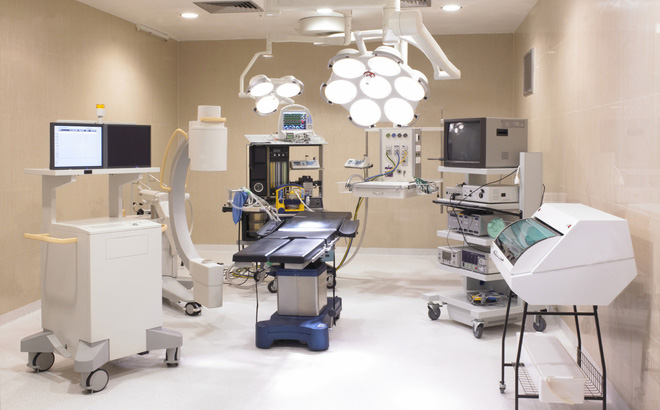
Trình tự, thủ tục cho phép áp dụng chính thức kỹ thuật mới trong KCB (Hình minh họa)
Theo đó, Thông tư 07/2015/TT-BYT hướng dẫn trình tự, thủ tục cho phép áp dụng chính thức kỹ thuật mới, phương pháp mới trong khám bệnh, chữa bệnh như sau:
- Cơ sở khám bệnh, chữa bệnh nộp 01 bộ hồ sơ theo quy định tại Điều 11 Thông tư này về cơ quan tiếp nhận hồ sơ theo quy định tại Điều 8 Thông tư này.
- Hình thức nộp hồ sơ: Nộp trực tiếp tại cơ quan tiếp nhận hồ sơ hoặc gửi qua đường bưu điện.
- Trong thời hạn 05 ngày làm việc, kể từ ngày nhận hồ sơ (căn cứ vào ngày ghi trên sổ công văn đến của cơ quan tiếp nhận hồ sơ), cơ quan tiếp nhận hồ sơ phải xác định hồ sơ hợp lệ hoặc chưa hợp lệ.
-
Đối với hồ sơ chưa hợp lệ, cơ quan tiếp nhận hồ sơ phải có văn bản thông báo cho cơ sở khám bệnh, chữa bệnh đề nghị áp dụng chính thức kỹ thuật mới, phương pháp mới hoàn chỉnh hồ sơ. Văn bản thông báo phải nêu cụ thể tài liệu, nội dung cần sửa đổi, bổ sung.
-
Khi nhận được văn bản yêu cầu hoàn chỉnh hồ sơ, cơ sở khám bệnh, chữa bệnh phải bổ sung, sửa đổi theo đúng những nội dung đã được ghi trong văn bản và gửi về cơ quan tiếp nhận hồ sơ, ngày tiếp nhận hồ sơ sửa đổi, bổ sung được ghi trên Phiếu tiếp nhận hồ sơ hoặc Sổ công văn đến của cơ quan tiếp nhận hồ sơ, trường hợp hồ sơ bổ sung vẫn không đạt thì cơ sở khám bệnh, chữa bệnh phải tiếp tục hoàn thiện hồ sơ.
- Trong thời hạn 15 ngày làm việc, kể từ ngày nhận đủ hồ sơ hợp lệ được ghi trên Phiếu tiếp nhận hồ sơ hoặc Sổ công văn đến:
-
Đối với các kỹ thuật mới, phương pháp mới quy định tại Điểm b Khoản 1, Khoản 2 Điều 2 Thông tư này: Cục trưởng Cục Quản lý Khám, chữa bệnh phải quyết định thành lập Hội đồng chuyên môn và tổ chức thẩm định kết quả triển khai thí điểm và quy trình kỹ thuật do cơ sở khám bệnh, chữa bệnh đề xuất.
-
Đối với các kỹ thuật mới, phương pháp mới quy định tại Khoản 3 Điều 2 Thông tư này: Cục trưởng Cục Quản lý Khám, chữa bệnh hoặc Giám đốc Sở Y tế phải quyết định thành lập Hội đồng chuyên môn và tổ chức thẩm định kết quả triển khai thí điểm và quy trình kỹ thuật do cơ sở khám bệnh, chữa bệnh đề xuất.
- Hội đồng chuyên môn quy định tại Khoản 4 Điều này bao gồm: các chuyên gia trong các lĩnh vực quản lý, lâm sàng, cận lâm sàng có liên quan đến kỹ thuật mới, phương pháp mới. Hội đồng chuyên môn có trách nhiệm thẩm định kết quả triển khai thí điểm, quy trình kỹ thuật và có kết luận bằng biên bản.
- Trong thời hạn 05 ngày làm việc, kể từ ngày nhận được biên bản thẩm định của Hội đồng chuyên môn, Bộ trưởng Bộ Y tế hoặc Giám đốc Sở Y tế quyết định cho phép cơ sở khám bệnh, chữa bệnh triển khai chính thức áp dụng kỹ thuật mới, phương pháp mới và phê duyệt quy trình kỹ thuật. Trường hợp không đồng ý phải có văn bản trả lời và nêu rõ lý do.
Chi tiết xem tại Thông tư 07/2015/TT-BYT, có hiệu lực từ 01/06/2015
Lê Hải
- Từ khóa:
- Thông tư 07/2015/TT-BYT
- Yêu cầu kỹ thuật công tác thăm dò cát, sỏi lòng sông và đất, đá làm vật liệu san lấp từ ngày 06/6/2024
- Công khai thông tin về kế toán viên hành nghề từ ngày 01/7/2024
- Đề xuất sửa đổi quy định đối tượng tham gia bảo hiểm thất nghiệp
- Đề xuất chính sách hỗ trợ người lao động đi làm việc ở nước ngoài theo hợp đồng
- Triển khai hoạt động kích cầu du lịch nội địa năm 2024
- Kế hoạch thực hiện công tác Dân quân tự vệ, giáo dục quốc phòng năm 2024 của Bộ Tư pháp
-

- Hồ sơ đề nghị áp dụng thí điểm kỹ thuật, phương ...
- 10:52, 06/04/2015
-

- 04 điều kiện áp dụng kỹ thuật mới, phương pháp ...
- 10:43, 06/04/2015
-
- 02 nguyên tắc chung về áp dụng kỹ thuật mới, phương ...
- 09:57, 06/04/2015
-

- Hướng dẫn cách xác định kỹ thuật mới, phương pháp ...
- 09:47, 06/04/2015
-

- 06 thủ tục hành chính nội bộ lĩnh vực địa chất ...
- 16:11, 23/04/2024
-
- Bảo đảm công tác cấp cứu tai nạn giao thông trong ...
- 16:03, 23/04/2024
-

- Công khai thông tin về kế toán viên hành nghề ...
- 16:00, 23/04/2024
-

- Chính sách của Nhà nước về chăn nuôi
- 15:01, 23/04/2024
-

- Đề xuất sửa đổi quy định đối tượng tham gia bảo ...
- 14:41, 23/04/2024
 Mục lục bài viết
Mục lục bài viết
